2017上海中考英语:2017上海中考:初中化学碳及其化合物知识点
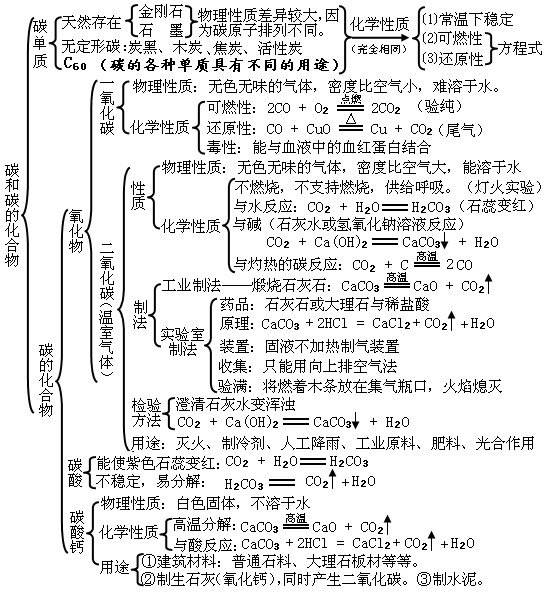
1. 单质碳的化学性质:
C:还原性:
C + 2CuO 2Cu + CO2↑ (置换反应)
现象:黑色粉末逐渐变成光亮红色,产生的的气体能使澄清的石灰水变浑浊。
C在反应中得到氧元素,发生氧化反应,是还原剂,具有还原性。
CuO在反应中失去氧元素,发生还原反应,是氧化剂。具有氧化性。
小结:还原剂:夺去氧元素的物质,具有还原性。得到氧元素,发生氧化反应。
氧化剂:提供氧元素的物质,具有氧化性。失去氧元素,发生还原反应。
应用:冶金工业:
2Fe2O3+3C 4Fe+3CO2↑ C+CO2 2CO
2.二氧化碳的制法:
(1)工业上制取二氧化碳:
煅烧石灰石: CaCO3高温CaO+CO2↑
而本实验是固体和液体之间进行反应,所以采取的装置图如下:
装置的注意事项:若用长颈漏斗来注入盐酸,长颈漏斗下端必须伸入液面以下,防止因为压强差的原因导致稀硫酸喷出。
(4)二氧化碳的收集:气体的收集方法主要是由气体的物理化学性质决定的,难溶于水用排水法收集,密度比空气大用向上排空气法。
由于CO2易溶于水,密度比空气小,所以只能用:向上排空气法
(5)二氧化碳的验满方法是:用点燃的木条,放在集气瓶口,木条熄灭。证明已集满二氧化碳气体。
3.二氧化碳的性质:
(1) 二氧化碳的物理性质:无色,无味的气体,密度比空气大,能溶于水,高压低温下可得干冰,不支持燃烧。
(2) 二氧化碳的化学性质:
A:一般情况下不能燃烧,也不支持燃烧,不能供给呼吸
B:与水反应生成碳酸: CO2+H2O==H2CO3 生成的碳酸能使紫色的石蕊试液变红,
碳酸不稳定,易分解:H2CO3 == H2O+ CO2↑
所以如果产物里有碳酸生成的时候,一般写成H2O+ CO2↑
4.二氧化碳的用途:
① 灭火(灭火器原理:Na2CO3+2HCl==2NaCl+H2O+CO2↑,同时二氧化碳不支持燃烧)
② 干冰用于人工降雨、制冷剂(利用干冰升华时要吸收大量的热)
③ 温室肥料
④ 做碳酸型饮料(利用二氧化碳能溶于水)
5.温室效应:
(1)定义:由于人类消耗的能源急剧增加,森林遭到破坏,大气中的二氧化碳的量大量增加,使得地面吸收的太阳光的热量不易散失,从而使全球变暖,这种现象叫做温室效应。
(2)产生温室效应的物质:主要物质是二氧化碳
(3)产生温室效应的原因:人类消耗的能源急剧增加,森林遭到破坏
(4)减轻温室效应的措施:减少化石燃料的燃烧;植树造林;使用清洁能源
6.一氧化碳的性质:
(1)物理性质:无色,无味的气体,密度比空气略小,难溶于水,吸进肺里与血液中的血红蛋白结合,使人体缺少氧气而中毒
(2)化学性质:
A:可燃性:2CO+O2 2CO2
实验现象:发出蓝色火焰
B:还原性: CO+CuO △ Cu+CO2 (非置换反应)
现象:黑色的氧化铜逐渐变成光亮红色,产生的气体能使澄清的石灰水变浑浊。
Fe2O3+3CO 2Fe+3CO2
现象:红色粉末逐渐变成黑色,产生的气体能使澄清的石灰水变浑浊。
C:H2、CO、C具有相似的化学性质:
A)可燃性 C + O2 CO2 2CO+O2 2CO2 2H2 + O2 2H2O
B)还原性 :H2 + CuO Cu + H2O CO+CuO Cu+CO2
C + 2CuO 2Cu + CO2↑
2017上海中考:初中化学碳及其化合物知识点.doc正在阅读:
经典爱情祝福语短信201604-05
nginx伪静态规则写法05-29
2017年6月英语四级作文范文:洋快餐12-19
[2021中国自然资源航空物探遥感中心招聘18人公告]2021中国自然资源航空物探遥感中心招聘公告08-24
帝王故事之《刘备传艺》阅读08-16
忘不了的年味儿作文600字07-27